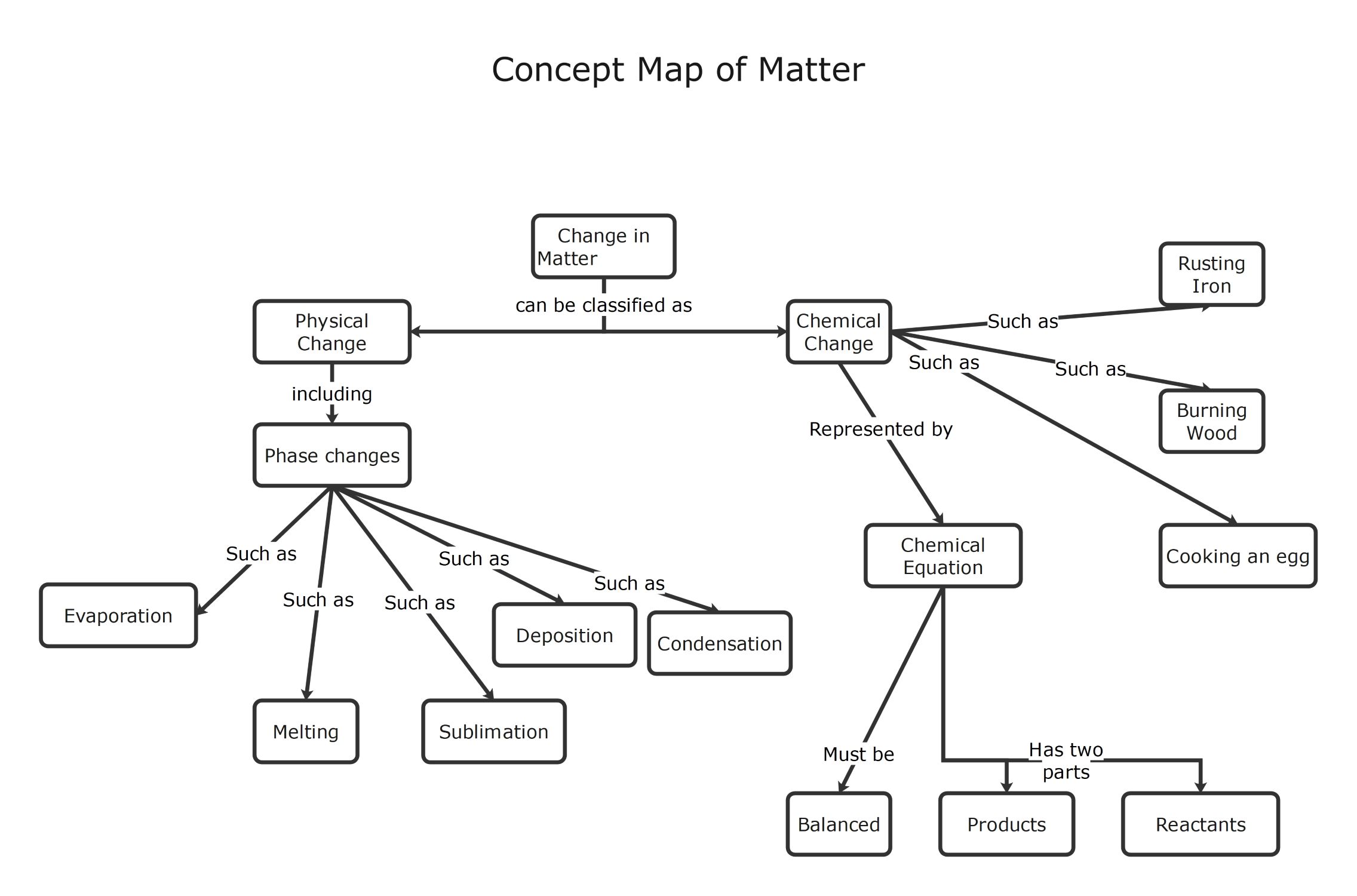
À propos de ce modèle de carte conceptuelle de la matière
Ce modèle sert de guide visuel pour comprendre les transformations de la matière. Il distingue clairement les changements physiques et chimiques. Les étudiants peuvent l'utiliser pour apprendre efficacement les changements de phase et les équations chimiques.
Changement physique
Les changements physiques impliquent des transformations qui ne modifient pas l'identité chimique d'une substance. Ils concernent généralement des transitions d'état où le matériau reste le même. Ces changements sont souvent réversibles et facilement observables.
- Évaporation
- Fusion
- Sublimation
- Déposition
- Condensation
Changement chimique
Les changements chimiques entraînent la formation de substances entièrement nouvelles avec des propriétés différentes. Ces processus impliquent la rupture ou la formation de liaisons. Ils sont généralement plus difficiles à inverser et produisent des signes observables spécifiques comme la chaleur ou la couleur.
- Oxydation du fer
- Combustion du bois
- Cuisson d'un œuf
Équation chimique
Une équation chimique représente la notation symbolique d'une réaction chimique. Elle montre comment les réactifs se transforment en produits tout en respectant la loi de conservation de la masse. La précision scientifique exige que ces équations soient parfaitement équilibrées.
- Équilibrée
- Produits
- Réactifs
FAQ concernant ce modèle
-
Comment identifiez-vous un changement physique dans la matière ?
Vous pouvez identifier un changement physique lorsque la substance semble différente mais reste la même au niveau moléculaire. Les exemples courants comprennent les changements de forme, de taille ou d'état, comme la glace qui fond en eau. Ces changements ne produisent pas de nouveaux produits chimiques. La plupart du temps, vous pouvez inverser un changement physique en modifiant simplement la température ou la pression de l'environnement.
-
Quels sont les principaux signes d'un changement chimique ?
Les changements chimiques produisent souvent des signes notables qu'une nouvelle substance s'est formée. Vous pourriez observer un changement de couleur, la production d'un gaz par des bulles, ou une odeur distincte. Dans de nombreux cas, ces réactions libèrent ou absorbent également de l'énergie, entraînant des changements de température ou de lumière. Contrairement aux changements physiques, les réactions chimiques sont généralement permanentes et ne peuvent pas être annulées par de simples moyens physiques.
-
Pourquoi une équation chimique équilibrée est-elle importante ?
Une équation chimique équilibrée est essentielle car elle obéit à la loi de conservation de la masse. Cette loi scientifique stipule que la matière ne peut être créée ni détruite pendant une réaction. Par conséquent, le nombre d'atomes pour chaque élément doit être égal des deux côtés. Cet équilibre garantit que l'équation représente fidèlement ce qui se passe dans la réalité lorsque les réactifs se transforment en produits lors d'un changement chimique.