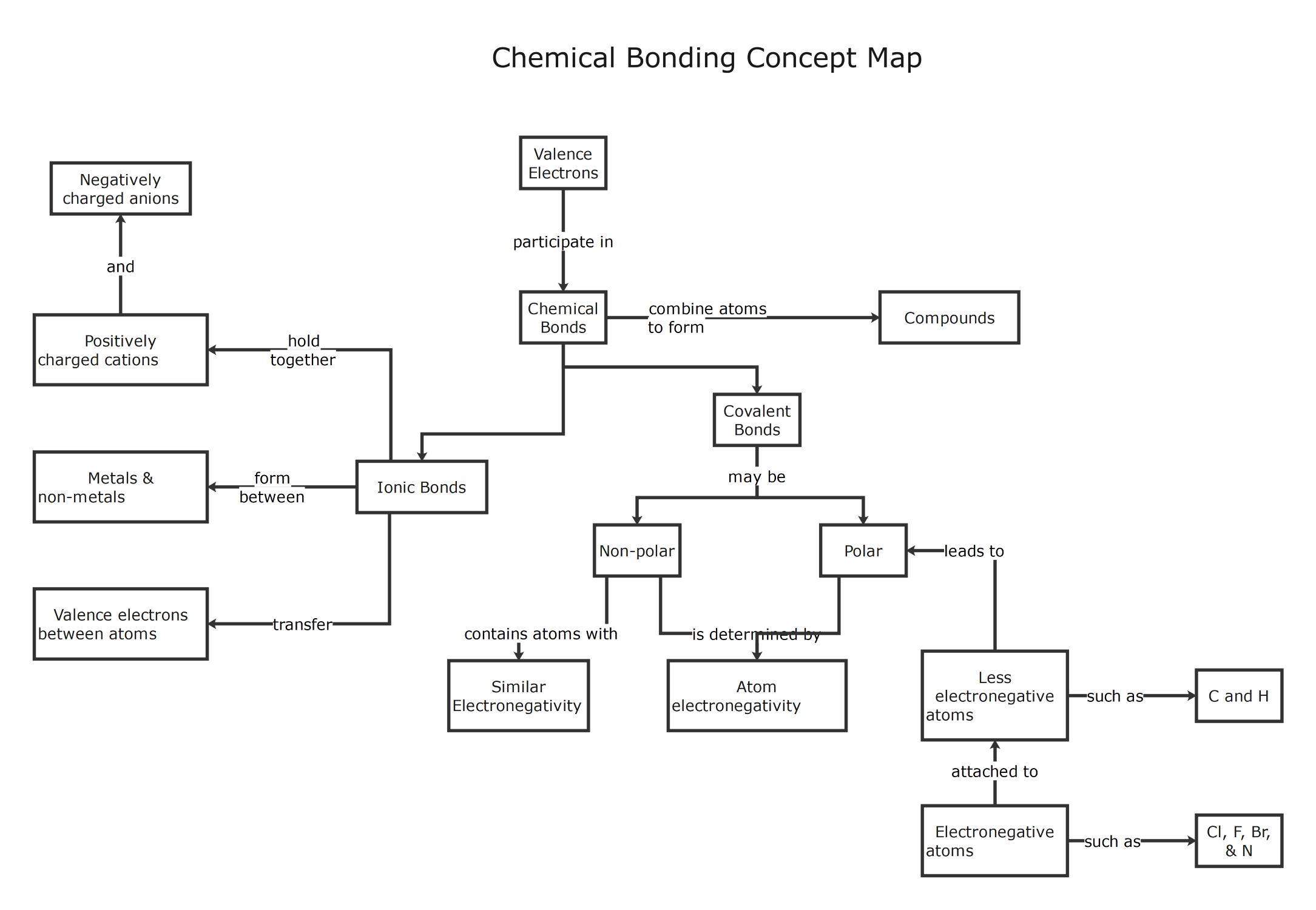
À propos de ce modèle de carte conceptuelle de liaison chimique
Ce modèle fournit un résumé visuel clair des façons dont les atomes interagissent à travers les électrons de valence. Il aide les étudiants et les éducateurs à cartographier les différences entre les liaisons ioniques et covalentes tout en soulignant les caractéristiques clés comme l'électronégativité et la charge.
Liaisons chimiques et électrons de valence
Les liaisons chimiques se forment lorsque les atomes interagissent par leurs électrons les plus externes pour atteindre la stabilité. Ce processus combine différents atomes pour créer des composés complexes qui sont les éléments constitutifs de toute matière trouvée dans l'univers.
- Électrons de valence
- Liaisons chimiques
- Composés
Liaisons ioniques et transfert d'électrons
Les liaisons ioniques se produisent lorsque les électrons se transfèrent entre atomes, impliquant généralement des métaux et des non-métaux. Cette attraction maintient ensemble des ions de charges opposées pour former des structures stables que l'on trouve souvent dans divers sels et minéraux courants.
- Cations chargés positivement
- Anions chargés négativement
- Métaux et non-métaux
- Transfert d'électrons de valence
Liaisons covalentes et électronégativité
Les liaisons covalentes impliquent le partage d'électrons entre atomes plutôt qu'un transfert complet. La nature de ce partage dépend fortement de l'électronégativité, qui détermine si la liaison résultante est classée comme polaire ou non polaire.
- Liaisons covalentes polaires
- Liaisons covalentes non polaires
- Électronégativité atomique
- Électronégativité similaire
Caractéristiques et exemples de liaisons polaires
Les liaisons polaires créent une distribution inégale d'électrons lorsqu'un atome électronégatif attire les électrons vers lui-même. Cette section met en évidence les éléments courants impliqués dans ces liaisons, tels que l'hydrogène et le carbone associés à des éléments halogènes hautement réactifs.
- Atomes moins électronégatifs (C et H)
- Atomes électronégatifs (Cl, F, Br et N)
- Partage inégal d'électrons
FAQ concernant ce modèle
-
Quelle est la différence entre les liaisons ioniques et covalentes ?
Les liaisons ioniques se forment lorsqu'un atome cède des électrons à un autre, créant des ions chargés qui s'attirent mutuellement. Cela se produit généralement entre les métaux et les non-métaux. En revanche, les liaisons covalentes impliquent des atomes qui partagent des électrons pour rester ensemble. Cela se produit le plus souvent entre des atomes non métalliques. Comprendre ces deux types de liaisons est essentiel pour prédire comment différentes substances se comporteront.
-
Comment l'électronégativité affecte-t-elle les liaisons chimiques ?
L'électronégativité mesure la force avec laquelle un atome attire les électrons. Si deux atomes ont des valeurs d'électronégativité très différentes, ils forment probablement une liaison ionique. Si les valeurs sont similaires, ils forment une liaison covalente non polaire. Cependant, s'il existe une différence modérée, une liaison covalente polaire se forme. Cela crée des charges partielles, qui influencent considérablement les propriétés physiques de la molécule résultante.
-
Pourquoi les électrons de valence sont-ils importants dans cette carte conceptuelle ?
Les électrons de valence sont les électrons spécifiques situés dans la couche la plus externe d'un atome. Ils sont les acteurs principaux dans les réactions chimiques et les liaisons. Comme ils sont les plus accessibles, ils déterminent comment un atome interagira avec ses voisins. La carte conceptuelle les met en évidence car tous les types de liaisons, qu'elles soient ioniques ou covalentes, reposent entièrement sur le comportement de ces électrons.