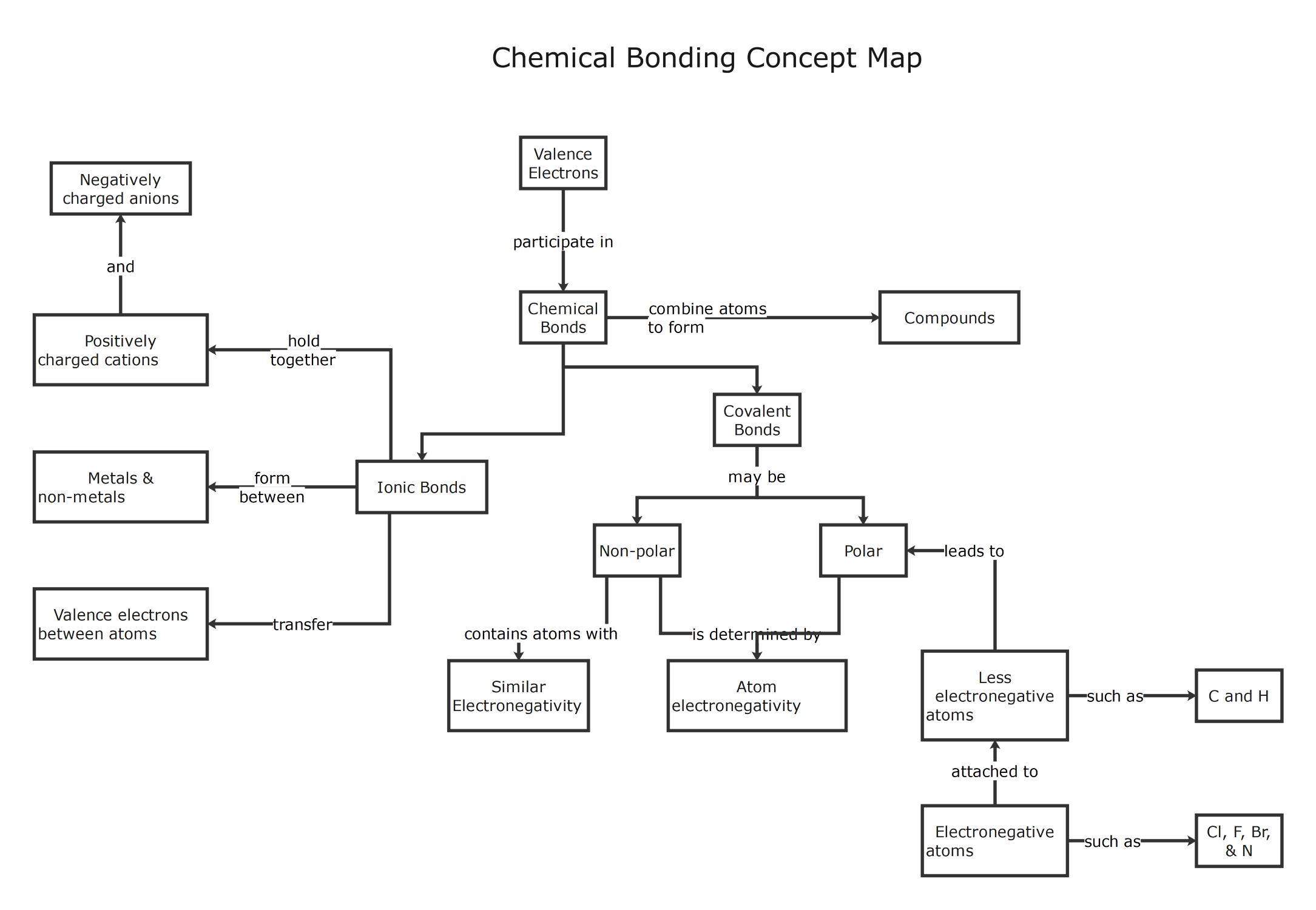
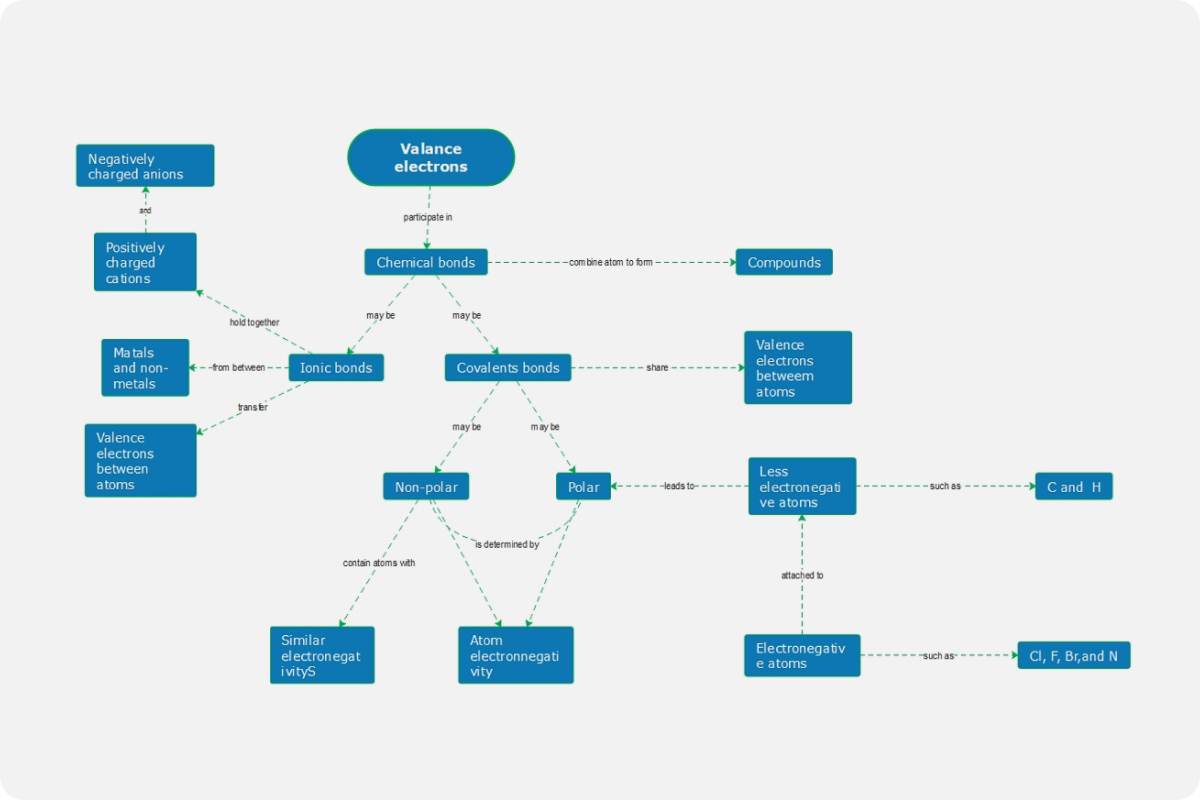
Über diese Konzeptkarte zur chemischen Bindung
Diese Vorlage bietet eine klare visuelle Zusammenfassung der Art und Weise, wie Atome über Valenzelektronen interagieren. Sie hilft Schülern und Lehrkräften, die Unterschiede zwischen Ionen- und Atombindungen zu strukturieren und dabei wichtige Merkmale wie Elektronegativität und Ladung hervorzuheben.
Chemische Bindungen und Valenzelektronen
Chemische Bindungen entstehen, wenn Atome über ihre äußersten Elektronen interagieren, um Stabilität zu erreichen. Dieser Prozess verbindet verschiedene Atome zu komplexen Verbindungen, die die Bausteine aller Materie im Universum bilden.
- Valenzelektronen
- Chemische Bindungen
- Verbindungen
Ionenbindungen und Elektronenübertragung
Ionenbindungen entstehen, wenn Elektronen zwischen Atomen übertragen werden, typischerweise zwischen Metallen und Nichtmetallen. Diese Anziehungskraft hält entgegengesetzt geladene Ionen zusammen und bildet stabile Strukturen, die häufig in verschiedenen Salzen und Mineralien vorkommen.
- Positiv geladene Kationen
- Negativ geladene Anionen
- Metalle und Nichtmetalle
- Übertragung von Valenzelektronen
Atombindungen und Elektronegativität
Atombindungen beruhen auf der gemeinsamen Nutzung von Elektronen zwischen Atomen anstelle einer vollständigen Übertragung. Die Art dieser Elektronenteilung hängt stark von der Elektronegativität ab, die bestimmt, ob die resultierende Bindung als polar oder unpolar klassifiziert wird.
- Polare Atombindungen
- Unpolare Atombindungen
- Elektronegativität der Atome
- Ähnliche Elektronegativität
Merkmale und Beispiele polarer Bindungen
Polare Bindungen erzeugen eine ungleiche Elektronenverteilung, wenn ein elektronegatives Atom Elektronen zu sich zieht. Dieser Abschnitt hebt häufig beteiligte Elemente in solchen Bindungen hervor, wie Wasserstoff und Kohlenstoff in Kombination mit hochreaktiven Halogenelementen.
- Weniger elektronegative Atome (C und H)
- Elektronegative Atome (Cl, F, Br und N)
- Ungleiche Elektronenteilung
FAQs zu dieser Vorlage
-
Was ist der Unterschied zwischen Ionen- und Atombindungen?
Ionenbindungen entstehen, wenn ein Atom Elektronen an ein anderes abgibt und dadurch geladene Ionen bildet, die sich gegenseitig anziehen. Dies geschieht typischerweise zwischen Metallen und Nichtmetallen. Im Gegensatz dazu teilen sich Atome bei Atombindungen (kovalenten Bindungen) Elektronen, um zusammenzuhalten. Dies tritt meist zwischen Nichtmetallatomen auf. Das Verständnis dieser beiden Bindungsarten ist wichtig, um vorherzusagen, wie sich verschiedene Stoffe verhalten werden.
-
Wie beeinflusst die Elektronegativität die chemische Bindung?
Elektronegativität misst, wie stark ein Atom Elektronen anzieht. Wenn zwei Atome sehr unterschiedliche Elektronegativitätswerte haben, bilden sie wahrscheinlich eine Ionenbindung. Bei ähnlichen Werten entsteht eine unpolare Atombindung. Bei einem moderaten Unterschied hingegen bildet sich eine polare Atombindung. Dadurch entstehen partielle Ladungen, die die physikalischen Eigenschaften des resultierenden Moleküls erheblich beeinflussen.
-
Warum sind Valenzelektronen in dieser Konzeptkarte wichtig?
Valenzelektronen sind die spezifischen Elektronen in der äußersten Schale eines Atoms. Sie sind die hauptsächlichen Akteure bei chemischen Reaktionen und Bindungen. Da sie am leichtesten zugänglich sind, bestimmen sie, wie ein Atom mit seinen Nachbaratomen interagiert. Die Konzeptkarte hebt sie hervor, weil alle Bindungsarten – ob ionisch oder kovalent – vollständig vom Verhalten dieser Elektronen abhängen.